皱纹卫生纸(QB 2500-2000)
2001-06-01实施
范围
本标准规定了皱纹卫生纸的产品分类、技术要求、试验方法、检验规则及标志、包装、运输、贮存等要求。
本标准适用于人们日常生活用的厕所卫生用纸。
产品分类
1 皱纹卫生纸按质量分为A、B、C、D、E等品。
2 皱纹卫生纸可分为小卷筒和平切两种型式。
技术要求
1 皱纹卫生纸的技术指标应该符合表1的规定。
2 按供需双方协定,可生产其它定量的皱纹卫生纸,抗张强度和柔软度指标按插入法换算。
3 小卷筒纸的卷高、卷重,平切纸的幅长、幅宽、包装重量,均应按订货合同规定。小卷筒纸的卷高尺寸偏差不得超过±2mm,偏斜度不超过2mm;卷纸重量负偏差不大于4%。平切纸幅长、幅宽规格尺寸偏差不超过±3mm,,偏斜度不超过3mm,平切纸包装重量负偏差不大于4%。
4 A、B等品皱纹卫生纸一般为双层。根据用户要求可生产其它层数的纸,其指标应符合表1规定。
5 可生产各种颜色的皱纹卫生纸,每批色泽不许有显著差别。
6 A、B等品小卷筒纸应打针孔,其节距可为135mm,140mm等,偏差±3mm,打孔应清晰、易断、整齐。
7 纸张皱纹应均匀、细腻。A、B等品皱纹卫生纸在同一纸幅内纵向不许有条形粗纹。
8 纸面不许有明显尘埃(或符合订货合同的具体规定)、死褶、硬质块、生草筋等纸病或杂质,不许有掉毛、掉粉、掉色现象。
9 皱纹卫生纸不得采用垃圾纸等含有病源微生物及有害物质的原料。
10 有下列情况者可列为二等品。但不得同时超过两项。
a)定量超过允许偏差2g/m2以内者;
b)亮度低于或高于规定2%(绝对值)以内者;
c)洞眼超过规定20%以内者(洞眼规定数量小于10个/m2,允许超过规定1个/m2);
d)柔软度超过规定10%以内者。
表1 技术指标
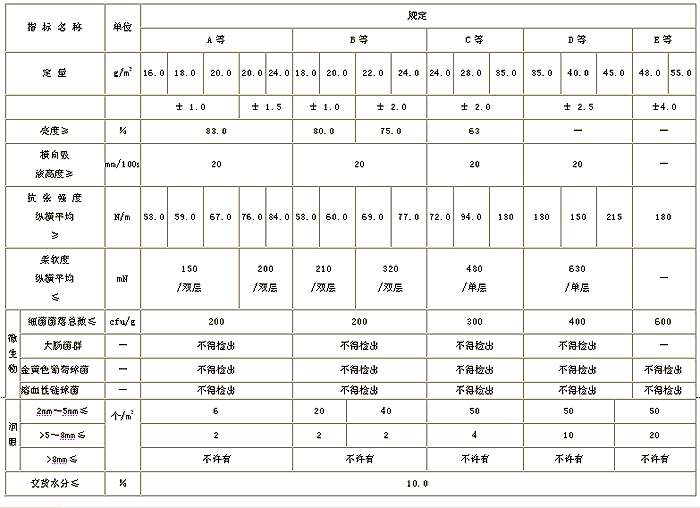
注:①表1中抗张强度、柔软度及微生物指标为强制性指标。
②用全苇浆生产的皱纹卫生纸横向吸液高度按5min考核。
检验方法
以下试验为检验加工包装后的最终产品。
1 试样的采取按GB/T450进行。
2 试样的处理按GB/T10739进行(物理性能测试),标准大气条件为(23±1)℃、(52±2)%r.h.。
3 平切纸幅长、幅宽及偏斜度、小卷筒纸的尺寸按GB/T451.1规定进行测定。
小卷筒纸偏斜度测定方法:取小卷筒皱纹卫生纸两节纸,以其针孔线为中心对折在一起,用尺量取两节纸边端的差距,按此方法量取5个试样,取其平均值,结果精确至1mm。
4定量 按GB/T451.2进行测定。
5 抗张强度按GB/T453或GB/T12914进行测定,仲裁时按GB/T12914进行。根据需要可以采用50mm试验夹距。双层或多层试样应以双层或多层测试,然后换算成单层的测定值。
6 亮度按GB/T7974或GB/T8940.1进行测定,仲裁时按GB/T7974进行测定。
7 横向吸液高度按GB/T461.1测定(单层)。
8 柔软度按GB/T8942,狭缝宽5mm。
9 微生物指标含细菌菌落总数、大肠菌群、金黄色葡萄球菌、溶血性链球菌,按附录A进行测定。
10 洞眼按附录B进行测定
11 交货水分按GB/T462进行测定。
检验规则
1 微生物指标为否决性指标,每季度进行一次检验,首件检验测定结果作为该季度微生物指标的检测结果,应符合表1的规定。
2 交收检验
2.1 以一次交货数量为一批,但不多于30t。
2.2 生产厂应保证生产的产品符合本标准的要求,每件(箱)纸交货时,应附有产品合格证。
2.3 产品交收检验按GB/T2828进行,交收检验项目及检查水平、抽样检查方案和合格质量水平(AQL)按表2进行。
表2
|
抽样方案 |
正常检查二次抽样方案 |
不合格分类 | |||||
|
样本大小 |
B类不合格品 |
C类不合格品 |
B类不合格品 |
C类不合格品 | |||
|
AQL=4.0 |
AQL=6.5 | ||||||
|
批量(件或箱) |
Ac |
Re |
Ac |
Re | |||
|
≤150 |
3 |
0 |
1 |
- |
- |
抗张强度 柔软度 |
定量 横向吸液高度 亮度 洞眼 交货水分 外观质量 |
|
5 |
- |
- |
0 |
2 | |||
|
5(10) |
- |
- |
1 |
2 | |||
|
150~3200 |
8 |
0 |
2 |
0 |
3 | ||
|
8(16) |
1 |
2 |
3 |
4 | |||
2.4 判定规则
若同时出现B类和C类不合格品时,在符合B类不合格品Ac,Re判定要求的前提下,同时只有在B类与C类不合格品之和小于或等于C类不合格品的Ac值时,则判为批合格,若大于则判为不合格。若小于C类不合格品的Re值且大于Ac值,则进行第二样本的测试和判定,判定方法同前。
3 微生物指标检验,有一项不合格判为批不合格。
4 需方有权按本标准的要求检验产品质量,如对产品质量有异议,应在到货后三个月内通知供方,双方共同抽样检验,如不符合本标准的规定,则判为批不合格,由供方负责处理;如符合本标准的规定,则判为批合格,由需方负责处理。
标志、包装、运输、贮存
1 每卷(包、袋)皱纹卫生纸应用塑料或包装,封口整齐牢固,不许有破损。
2 标志按国家技术监督局颁布的《产品标识标注规定》进行。
3 皱纹卫生纸运输时应采用洁净的运输工具,防止产品污染,搬运时不许将纸件从高处扔下,以防损坏外包装。。
4 皱纹卫生纸应存放于干燥、通风、洁净的地方妥善保管,以防雨、雪及潮湿侵入产品,影响质量。
5 由于保管和运输不符合本标准要求,产品发生变质或其它损坏,应由造成损坏的责任方负责。
附录A
(标准的附录)
(标准的附录)
微生物指标的测定法
A1培养基与试剂制备
A1.1 营养琼脂培养基
成分:
|
蛋白胨 |
10 g |
|
牛肉膏 |
3 g |
|
氯化钠 |
5 g |
|
琼脂 |
15 g |
|
蒸馏水 |
1 000 mL |
制法:除琼脂外其他成分溶解于蒸馏水中,调pH至7.2~7.4,加入琼脂,加热溶解,分装试管,121℃灭菌15 min后备用。
A1.2 乳糖胆盐发酵管
成分:
|
|
蛋白胨 |
20 g |
|
|
猪胆盐(或牛、羊胆盐) |
5 g |
|
|
乳糖 |
10 g |
|
|
0.04%溴甲酚紫水溶液 |
25 mL |
|
|
蒸馏水 |
加至1 000 mL |
制法:将蛋白胨、胆盐及乳糖溶于水中,校正pH至7.4,加入指示剂,分装每管10 mL,并放入一个小倒管,115℃灭菌15 min,即得。
注:双料乳糖胆盐管除蒸馏水外,其他成分加倍。
A1.3 伊红美蓝琼脂(EMB)
成分:
|
|
蛋白胨 |
10 g |
|
|
乳糖 |
10 g |
|
|
磷酸氢二钾 |
2 g |
|
|
琼脂 |
17 g |
|
|
2%伊红溶液 |
20 mL |
|
|
0.65%美蓝溶液 |
10 mL |
|
|
蒸馏水 |
加至1 000 mL |
制法:将蛋白胨、磷酸盐和琼脂溶解于蒸馏水中,校正pH至7.1,分装于烧瓶内,121℃灭菌15 min备用,临用时加入乳糖并加热溶化琼脂,冷至50~60℃,加入伊红美蓝溶液摇匀,倾注平板。
A1.4 乳糖发酵管
成分:
|
|
蛋白胨 |
20 g |
|
|
乳糖 |
10 g |
|
|
0.04%溴甲酚紫水溶液 |
25 mL |
|
|
蒸馏水 |
加至1 000 mL |
制法:将蛋白胨及乳糖溶于水中,校正pH至7.4,加入指示剂,分装每管10 mL,并放入一个小倒管,115℃灭菌15 min,即得。
A1.5 SCDLP液体培养基
成分:
|
|
酪蛋白胨 |
17 g |
|
|
大豆蛋白胨 |
3 g |
|
|
氯化钠 |
5 g |
|
|
磷酸氢二钾 |
2.5 g |
|
|
葡萄糖 |
2.5 g |
|
|
卵磷脂 |
1 g |
|
|
吐温80 |
7 g |
|
|
蒸馏水 |
1 000 mL |
制法:将各种成分混合(如无酪蛋白胨和大豆蛋白胨可用日本多胨代替),加热溶解,调pH至7.2~7.3,分装,121℃灭菌20 min,摇匀,避免吐温80沉于底部,冷至25℃后使用。
A1.6 血琼脂培养基
成分:
|
|
营养琼脂 |
100 mL |
|
|
脱纤维羊血(或兔血) |
10 mL |
制法:将营养琼脂加热溶化,待凉至50℃左右以无菌操作将10 mL脱纤维血加入后摇匀,倒平皿置冰箱备用。
A1.7 甘露醇发酵培养基
成分:
|
|
蛋白胨 |
10 g |
|
|
牛肉膏 |
5 g |
|
|
氯化钠 |
5 g |
|
|
甘露醇 |
10 g |
|
|
0.02%溴麝香草酚蓝溶液 |
12 mL |
|
|
蒸馏水 |
1 000 mL |
制法:将蛋白胨、氯化钠、牛肉膏加到蒸馏水中,加热溶解,调pH至7.4,加入甘露醇和溴麝香草酚蓝混匀后,分装试管,115℃灭菌20 min备用。
A1.8 兔血浆
制法:取灭菌3.8%柠檬酸钠1份,加兔全血4份,混匀静置,3 000 r/min离心5 min,取上清,弃血球。
A1.9 匹克氏肉汤
成分:
|
|
含1%胰蛋白胨的牛心浸液 |
200 mL |
|
|
1∶25 000结晶紫盐水溶液 |
10 mL |
|
|
1∶800三氮化钠溶液 |
10 mL |
|
|
脱纤维兔血(或羊血) |
10 mL |
制法:上述各成分无菌处理后用无菌操作混合,分装灭菌试管,每管2 mL,冰箱保存备用。
A1.10 革兰氏染色液
结晶紫染色液:
|
|
结晶紫 |
1 g |
|
|
95%酒精 |
20 mL |
|
|
1%草酸铵水溶液 |
80 mL |
将结晶紫溶解于酒精中,然后与草酸铵溶液混合。
革兰氏碘液:
|
|
碘 |
1 g |
|
|
碘化钾 |
2 g |
|
|
蒸馏水 |
300 mL |
将碘与碘化钾先进行混合,加入蒸馏水少许,充分振摇,待完全溶解后,再加蒸馏水至300 mL。
沙黄复染液:
|
|
沙黄 |
0.25 g |
|
|
95%酒精 |
10 mL |
|
|
蒸馏水 |
90 mL |
将沙黄溶解于酒精中,然后用蒸馏水稀释。
A2 产品采集与样品处理
于同一批号的三个大包装中至少随机抽取15包小包装样品,三分之一用于测试,三分之一留样,三分之一必要时复测用。样品最小包装不应有破裂,检验前不得启开。
在100级净化条件下或超净工作台中用无菌方法至少打开5个小包装,从中随机准确称取10 g样品,剪碎后加入到100 mL灭菌生理盐水中,振打80次或用混匀器充分混匀。每一种样品共取30 g,分别接种3管生理盐水样液。
A3 细菌菌落总数测试方法
A3.1操作步骤
待上述样液自然沉降后取上清液作菌落计数。共接种6个平皿,每个平皿中加入1 mL样液,然后用冷却至45℃左右的熔化的营养琼脂15 mL倒入平皿内,混合均匀。待琼脂凝固后翻转平皿置37℃ 培养24 h后,计算平板上的菌落数。当平板上菌落数超过300时应稀释后再计数。
A3.2 菌落计数及结果报告
菌落呈片状生长的平板不宜采用;计数符合要求的平板上的菌落,按式(A1)计算结果:
每克样品细菌菌落总数(cfu/g)=平板上菌落平均数×10 (A1)
所得结果超过标准值的10%,必须重复检测一次,以两次结果的平均数为最终结果。
当菌落数在100以内时,按实有数报告,大于100时采用二位有效数字。
A4 大肠菌群检测方法
A4.1 操作步骤
取样液的上清液接种乳糖胆盐发酵管。共接种3管,每管接种1 mL样液,置37℃ 培养24 h,如不产酸也不产气,则报告为大肠菌群阴性。
如产酸产气,则划线接种伊红美蓝琼脂平板,置37℃ 培养18~24 h,观察平板上菌落形态。典型的大肠菌落为黑紫色或红紫色,圆形,边缘整齐,表面光滑湿润,常具有金属光泽,也有的呈紫黑色,不带或略带金属光泽,或粉紫色,中心较深的菌落。
挑取可疑大肠菌落1~2个进行革兰氏染色镜检,同时接种乳糖发酵管于37℃培养24 h,观察产气情况。
A4.2 结果报告
凡乳糖胆盐发酵管产酸产气,乳糖发酵管产气,在伊红美蓝平板上有典型大肠菌落,革兰氏染色为阴性无芽胞杆菌,可报告被检样品检出大肠菌群。
A5 金黄色葡萄球菌检测方法
A5.1 操作步骤
取样液5 mL,加入到50 mL SCDLP培养液中,充分混匀,置37℃培养24 h。
自上述增菌液中取1~2接种环,划线接种在血琼脂培养基上,置37℃培养24~48 h。在血琼脂平板上该菌菌落呈金黄色,大而突起,圆形,不透明,表面光滑,周围有溶血圈。
挑取典型菌落,涂片作革兰氏染色镜检。金黄色葡萄球菌为革兰氏阳性球菌,排列成葡萄状,无芽胞与荚膜。镜检符合上述情况,应进行下列试验:
甘露醇发酵试验:取上述菌落接种到甘露醇培养液中,置37℃培养24 h,发酵甘露醇产酸者为阳性。
血浆凝固酶试验
玻片法:取清洁干燥载玻片,一端滴加一滴生理盐水,另一端滴加一滴兔血浆,挑取菌落分别与生理盐水和血浆混合,5 min如血浆内出现团块或颗粒状凝块,而盐水滴仍呈均匀混浊无凝固则为阳性,如两者均无凝固则为阴性。凡盐水滴与血浆滴均有凝固现象,再进行试管凝固酶试验。
试管法:吸取1∶4新鲜血浆0.5 mL,放灭菌小试管中,加入等量待检菌24 h肉汤培养物0.5 mL。混匀,放37℃温箱或水浴中,每半小时观察一次,24 h之内呈现凝块即为阳性。同时以已知血浆凝固酶阳性和阴性菌株肉汤培养物各0.5 mL作阳性与阴性对照。
A5.2 结果报告:凡在琼脂平板上有可疑菌落生长,镜检为革兰氏阳性葡萄球菌,并能发酵甘露醇产酸,血浆凝固酶试验阳性者,可报告被检样品检出金黄色葡萄球菌。
A6 溶血性链球菌检测方法
A6.1 操作步骤
取样液5 mL加入到50 mL匹克氏肉汤(A1.9)中,37℃培养24 h。
将培养物划线接种血琼脂平板,37℃培养24 h观察菌落特征。溶血性链球菌在血平板上为灰白色,半透明或不透明,针尖状突起,表面光滑,边缘整齐,周围有无色透明溶血圈。
挑取典型菌落作涂片革兰氏染色镜检,应为革兰氏阳性,呈链球状排列的球菌。镜检符合上述情况,应进行下列试验:
链激酶试验:吸取草酸钾血浆0.2 mL(0.01 g草酸钾加5 mL兔血浆混匀,经离心沉淀,吸取上清液),加入0.8 mL灭菌生理盐水,混匀后再加入待检菌24 h肉汤培养物0.5 mL和0.25%氯化钙0.25 mL,混匀,放37℃水浴中,2 min观察一次(一般10 min内可凝固),待血浆凝固后继续观察并记录溶化时间。如2 h内不溶化,继续放置24 h后观察,如凝块全部溶化为阳性,24 h仍不溶化为阴性。
杆菌肽敏感试验:将被检菌菌液涂于血平板上,用灭菌镊子取每片含0.04单位杆菌肽的纸片放在平板表面上,同时以已知阳性菌株作对照,在37℃下放置18~24 h,有抑菌带者为阳性。
A6.2 结果报告:镜检革兰氏阳性链状排列球菌,血平板上呈现溶血圈,链激酶和杆菌肽试验阳性,可报告被检样品检出溶血性链球菌。
附录B
(标准的附录)
洞眼测定法
(标准的附录)
洞眼测定法
B1 取单层纸样于眼前迎光观测,按标准规定数取各范围内的洞眼个数。半透明眼(洞眼间有纤维连接)不予计数。
B2 每份样品测试不少于0.5m2,然后换算成每平方米的洞眼数,计算结果取整数。
B3 大于8mm的洞眼取5m2进行测定。

 电话:010-64778188
电话:010-64778188  Email:cidpex@cnppri.com 地址:北京市朝阳区启阳路4号院2号楼
Email:cidpex@cnppri.com 地址:北京市朝阳区启阳路4号院2号楼 公众微信号
公众微信号